에이치엘비 주가전망 Feat. 에이치엘비 주가상승이유

오늘 필자는 요즘 무섭게 주가 상승을 하고있는 에이치엘비 주가전망에 대해서 포스팅을 하도록 하겠다.




최근 에이치엘비는 자회사 화진메디칼이 생산하는 주사기 ‘소프젝’(Sofjec)이 최근 미국 식품의약국(FDA)에서 승인(fast track)받았다고 밝혔다. 소프젝은 LDS(Low Dead Space·최소 잔여형) 기능이 탑재돼 백신의 낭비 없이 더 많은 사람들에게 백신을 접종할 수 있다. 승인에 따라 화진메디칼은 미국 의료기기 유통 전문업체 AMTC를 통해 미 연방정부에 주사기를 공급할 예정이다. 화진메디칼 이우준 사장은 "이번 승인을 통해 그동안 국내 시장에 주력했던 당사 제품이 미국을 포함한 전 세계에 수출될 수 있을 것으로 보인다"며 "향후 에이치엘비가 글로벌 권리를 확보한 코로나 백신 ‘나노코박스’의 접종에도 쓰일 것으로 보인다"고 말했다.
1. 에이치엘비 개요

HLB와 Elevar와 Immunomic 은 다양한 신약개발(항암제, 면역치료제 등) 및 임상실험 등의 경험을 보유하고 있는 글로벌 바이오 의약품 전문회사이다.
앞으로도 HLB는 지속적인 혁신과 끊임없는 도전을 통하여 인류의 건강과 보다 안전한 미래를 책임지고 이끌어 나갈 계획이다. 2020년 1월, HLB는 신규 Pipeline 확보를 위해 미국 면역치료플랫폼 바이오의약품 연구개발기업 Immunomic Therapeutics, Inc.("ITI")의 지분 2백만주를 미화 1천만불에 최초 취득하였고, 2020년 4월 지분 6백만주를 미화 3천만불, 2020년 12월 지분3,285,646주를 미화 약1.6천만불에 추가 취득하였다. HLB는 ITI의 Pipeline을 통하여기존 Pipeline인 Rivoceranib 성분 항암 신약 외에 각종 종양 및 알레르기에 대한 면역치료제 사업에 진출할 계획이다. 2020년 3월, Elevar는 스웨덴 바이오기업 Oasmia Pharmaceutical AB로부터 세포독성항암제인 파클리탁셀(Paclitaxel) 성분의 3세대 개량신약 항암제 "아필리아(Apealea)"에 대한 러시아, 북유럽과 동유럽 일부 국가를 제외한 글로벌 권리를 양수하였다. 아필리아는 2020년 1월 유럽에서 난소암 치료제로 공식 시판허가를 받은 약물로, 2021년 하반기부터 유럽 매출이 발생할 것으로 예상된다.
복합소재사업본부
1975년 설립 이후 지난 40여 년간 구명정, 관공선, 어업지도선 등 7000여 척의 선박을건조한 기술과 경험을 보유하여 국내 소형ㆍ특수선박 제작 분야에서는 가장 오랜 역사와 독보적인 노하우를 가지고 있으며, 2020년 6월에는 중소벤처기업부로부터 '친환경선박용 수소연료전지 추진 소형선박 제작과제'의 사업자로 선정되는 등 친환경 선박의 개발 및 상용화에 앞장서고 있다. 또한 해양플랜트, 발전소 등에 사용되는 유리섬유강화파이프(GRE/GRP Pipe)를 국내최초로 국산화하여 국내외 대형 중공업ㆍ화학업체에 공급하는 등 높은 기술력을 인정받고 있다.
Elevar Therapeutics Inc.
2005년 설립 이후 연구 단계나 초기 임상 단계의 물질을 도입하여 항암 신약을 개발하는 미국 소재 항암제 전문기업으로 에이치엘비가 지분 100%를 보유하고 있다. 혈관내피세포수용체(VEGFR-2)를 선택적으로 차단하는 경구용 표적항암제 리보세라닙(Rivoceranib)을 위암, 간암, 대장암, 선양낭성암 등 다양한 암종에 대한 치료제로 개발하고 있으며, 유럽에서 난소암 치료제로 품목허가를 받은 파크리탁셀의 3세대 개량신약 아필리아(Apealea)를 난소암, 유방암 등에 대한 치료제로 개발하고 있다.
Immunomic Therapeutics Inc.
2006년 설립 이후 핵산 면역 치료 플랫폼 연구를 개척하는 미국 소재 생명공학 회사로 에이치엘비가 지분 41.27%를 보유하고 있다. 미국 존스 홉킨스 대학과 협업을 바탕으로 개발한 차세대 면역치료 플랫폼 'UNITE'를 기반으로 특정항원을 리소좀에 타겟하여 항원제시능력을 높여 세포독성 T세포의 기능을 강화시키는 치료백신을 개발하고 있으며, 현재 미국에서 교모세포종에 대한 임상 2상이 진행되고 있다.
화진메디칼, 화진메디스
1993년 설립된 바이오 의료기기 전문 제조업체로 국내 주사기 제조 시장의 20~25%를 점유하고 있다. 'Sofjec(소프젝)'이라는 상표하에 일회용주사기, 필터주사기, 일회용주사침 등을 제조, 판매하고 있으며 에이치엘비가 지분 100%를 보유하고 있다. 2020년 9월, Advenchen Laboratories Nanjing, Ltd.과 SFFT Developing Co, Ltd.(이하 "양도인")와 자산양수도계약을 체결하고 양도인이 보유하고 있는 YN968D1(글로벌은 리보세라닙(Rivoceranib), 중국은 아파티닙(Apatinib)으로 명명)의 글로벌 특허권을 거래금액 4,200만불에 양수하기로 하였다. 해당 양수대금은 2020년 12월 4일에 지급하였다. 본 자산양수도로 리보세라닙의 글로벌 로열티 수령을 통한 장기적이고 안정적인 캐시플로우 및 영업이익을 확보하고, 항서제약과의 긴밀한 협력관계를 통하여 현재 진행중인 NDA와 리보세라닙의 추가 적응증 임상시험에 속도가 날 것으로 전망된다. 2020년 12월 리보세라닙 양도인인 Advenchen Laboratories Nanjing, Ltd.와 SFFT Developing Co., Ltd.는 당사의 제3자배정 유상증자에 참여, 당사 주식 295,950주를 취득하였으며 해당 주식은 전량 1년간 보호예수(2020.12.21~2021.12.21)되었다.
2. 에이치엘비 주요 제품 및 서비스

구명정 - 인명구조용
일반형 - 가장 대표적인 구명정으로 데빗에 의해 진수할 수 있으며, SOLAS규정을모두 만족하게 만들어졌으며, 위기발생시 신속한 탈출이 가능한 구조로 25인승부터 100인승까지 19개 모델을 보유하고 있어 선박의 규모에 따라 선택적용 가능
자유낙하식 - 선박의 선미에 탑재되어 자유낙하 방식으로 진수되는 구명정으로 2007년 5월 이후부터 건조되는 모든 Bulk Carrier선박에 설치가 의무화 되어있으며, 일반형 구명정의 진수 시 Davit Winch를 이용하는 방식 때문에 비상탈출 시간이 많이 소요되는 점과 본선의 양쪽에 각 한대 씩 설치되는 방식으로 인해 Deck House의 공간을 적절히 활용할 수 없는 점으로 인해 최근 자유낙하식 구명정을 선호하는 추세
구조정 - 선박의 선미에 장착하여 모선의 응급상황시 구조임무에 사용되는 보트로 보트 자유낙하식 구명정과 레스큐보트가 각 하나씩 한세트로 선박에 설치
특수선
관공선(인명구조 및 불법어업 단속) - 대형선박, 어업지도선, 해경경비정 등 선미데크에 설치되어 작업 및 신속한 인명구조활동 및 불법어업단속 등에 사용
도선선(도선사 선박 승,하선용) - 선박이 입출항하는 항만에서 도선사들이 선박을 탑승 및 하선을 위해 사용됨으로 이동시 실내 편의성, 속도, 선박 탑승시 안전성이 많이 요구되어 진다
유도선(여객선, 유람선, 도선) - 유선은 일반적으로 유람선을 의미하며 도선은 강과 바다가 접하는 하구 또는 만의 형태를 갖춘 곳으로 양 해안을 오가는 선박이며 선령 교체시기에 따라 비정기적으로 발주되는 선박임
GRP/GRE PIPE - 밸러스트 라인, 해수관,소화배관,냉각수관, 상하수도관 등
유리섬유로 강화된 플라스틱이라는 의미의 것으로 통상 강화플라스틱이라 하며, 철근과 콘크리트가 복합되어 좋은 강도를 얻는 것과 같이 내수,내약, 내열성이 좋은 수지를 혼합하여 사용되어 내구성, 강도, 내부식성의 이점을 모두 가짐
DAVIT - 선외 물체를 올리고 내리기 위한 기둥
선외 물체를 올리고 내릴 때 그 물체가 선체에 부딪치는 일없이 작업하기 편리하게 회전할 수 있게 되어 있음
주사기
일회용주사기(안정용) - 주사기는 인체 주사액 주입 시 사용되는 의료기기이며 일회용 주사기와 멸균주사침을 체결하여 사용하는 한벌 구성 의료기기로 1회에 한하여 사용하고 버리는 주사기다
멤브레인 필터주사기(약물주입, 앰플의 유리조각 제거, 바이알의 고무파편 제거, 기타 불순물 제거) -멤브레인 필터주사기 제품은 의약품주입여과기와 주사기로 구성된 의료기기로써, 혼합 액상의 약물 등을 주입 및/또는 흡인할 때 오염물질을 여과하기 위한 5.0㎛로 여과지(Filtration Membrane)가 부착된 침으로 1회용 멸균 의료기기이다. 사용목적 : 혼합 액상의 약물 등을 주입할 때 오염 물질을 걸러내는 기능
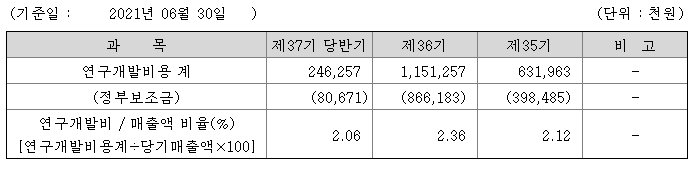
3. 에이치엘비 연구개발 활동
끊임없는 도전과 무한한 창조력으로 기술혁신의 새역사를 창조하는 기술연구소는 남보다 한 발 앞서가는 기술력과 최고의 제품을 향한 신념으로 미래를 개척하고 있다. 기술연구소의 주요업무로는 신제품 및 신기술 개발, 생산프로세스 개선신뢰성 있는 시험평가, 컴퓨터 시뮬레이션에 의한 사전 설계품질 검증 등을 추진하고 있다.
Elevar Therapeutics, Inc.
종속회사인 Elevar Therapeutics, Inc.의 연구개발 조직은 신약개발에 대한 연구를 진행하고 있다. 그 동안 표적항암제를 연구개발해 오면서 축적된 기술력과 노하우를 바탕으로 새로운 가치창조를 이루어 가고 있다.


Immunomic Therapeutics, Inc.
종속회사인 이뮤노믹(Immunomic Therapeutics, Inc.)의 연구개발 조직은 암, 알레르기 등 질환에 대한 핵산 면역치료 플랫폼(nucleic acid immunotherapy platforms)을 연구개발하고 있다. 이뮤노믹은 백신 디자인, 개발, 생산 및 시험에 대한 전문성을 바탕으로 암, 알레르기와 동물치료제에 대한 면역치료(immune therapy)가 가능한백신으로 인간의 삶을 변화시키고자 노력하고 있다.


5. 에이치엘비 사업의 추가설명




한국수출입은행 보고서상 글로벌 의약품 시장의 특징에 따르면, 신약개발은 많은 시간이 소요되고, 많은 자금이 투입되며 위험이 수반된다. 글로벌 신약 개발에는 수십억 달러 상당의 개발 비용과 약10년 이상의 예산과 기간이 소요된다고 한다. 신약개발의 단계는 후보물질 탐색, 비임상 실험, 임상시험 단계로 구분되며, 신약후보물질 검증을 위한 기초 R&D에 약 5년이 소요되며 이후 약 3년동안 비임상 단계에서 인간에게 약물을 투여하기 전에 동물대상으로 신약후보물질의 약물 효능 및 안전성 평가를 진행하게 되며 비임상 자료를 바탕으로 식약처에 IND((Investigational New Drug) 승인을 받고 임상단계에 진입하게 된다. 임상 단계는 최소6~7년가량이 소요되며, 임상시험 기관(병원)의 전문역량과 많은 비용이 소요되는 단계로 전체 신약개발 비용의 약 70%가량을 차지한다. 임상시험은 신약의 안전성과 유효성 입증을 위해 인간을 대상으로 실시하는 시험으로써, 총4상(Phase)으로 구성되며, 제I상(임상 1단계)에서는 소수의 건강한 성인을 대상으로 약물의 체내 흡수, 분포, 대사, 배설 등에 대한 약동학적인 자료를 수집하면서 안전성을 평가하게 되며(약 1~2년), 제II상(임상 2단계)에서는 수백명 가량의 해당질환을 보유한 환자들을 대상으로 투약용량의 범위와 용법을 평가하게 된다(약 2년), 제III상(임상 3단계)에서는 수천명의 해당질환 환자를 대상으로 약물의 유효성과안전성을 최종적으로 검증하게 되며(약 3년), 임상 3상을 통과하면 보건당국에 NDA(New Drug Application)를 신청하여 약물 제조 및 판매허가를 받게 된다. 보건당국으로부터 판매허가를 득한 후에 대규모 상용화 단계로 진입한다, 제IV상(임상 4단계)에서는 약물 허가 및 시판 후 부작용을 추적하여 안전성을 입증하고, 추가적 모니터링의 단계로 진행을 하게 된다. 타 산업 대비 연구개발 투자비율이 매우 높은 기술중심의 산업으로서, 연구개발비용 투입 상위기업 기준으로 매출액 대비 약20% 수준이며(일반제조업 약3%), 오랜 시간과 높은 비용이 소요되는 신약개발의 특성으로 인하여 중소업체 및 바이오벤처 등 소규모 기업이 신약개발 전 과정을 단독으로 진행하기 어렵다. 따라서, 높은 연구개발 투자 비용의 회수를 위해서는 큰 규모의 시장이 필요하여, 글로벌 진출 지향적인 산업구조를 가진다. 글로벌 의약품산업 연구개발 투자비는 2015~2022년 지속적으로 성장할 것으로 2022년 약 1,800억 달러의 규모를 형성할 것으로 예측된다(Evlaluate Pharma). 근래의 신약개발에 있어서 성공확률은 약1/5,000 수준으로 매우 낮은 상황이다. 기초 탐색단계에서 5,000~10,000개 수준의 화합물(Compound) 중 비임상 단계로 약250여개, 임상단계까지 5개, 최종 신약승인 허가를 득하고 최종단계인 상용화 단계에 도달하는 것은 1개 정도에 불과하다. 이와 같이 낮은 확률에도 불구하고 신약개발의 필요성이 대두되는 이유는 단 한 제품의 성공만으로도 글로벌 제약회사로 도약할 수 있으며, 특허 만료기간(약20년) 동안 물질특허를 인정받아 안정적으로 매출을 유지할 수 있다는 매력적인 장점을 가지고 있기 때문이다. 이처럼 하나의 글로벌신약으로 연간 수십억 달러 이상의의 매출을, 십 수 년간 독점적인 시장을 가지고 사업을 영위할 수 있는 산업이 바로 제약산업인 것이다.
전세계 처방의약품의 매출액 연평균 성장률은 2010∼2018년 약 2.3%였으나, 2019∼2024년 약 3배 정도 증가한 6.9%의 성장률이 전망되고 있다. 또한, 다양한 새로운기술의 출현은 제약산업 진화의 터닝포인트가 되어 될 것으로 예상되며, 특히 항암제분야의 경우 면역항암(Immuno-oncology) 계열의 확장은 제약산업 성장에 크게기여하며 기존의 세포독성항암제와 표적항암제와의 병용을 바탕으로 치료법의 발전과 더불어 시장을 확대하는데 큰 역할을 하고 있다. 특히 주목받는 치료영역으로는 시장 점유율 및 성장률이 높은 Oncology 분야의 지속강세 속에서 새로운 치료제 개발을 위한 연구개발도 활발하게 이루어지고 있다. 글로벌 제약시장 중에서 Oncology 분야의 매출 점유율이 가장 높으며(2018년 14.3%), 2024년까지의 성장률도 11.4%로 높은 수준을 예상하고 있으며 이에 따라 암 치료제(처방의약품+일반의약품) 매출은 2018년 1,238억 달러에서 2024년 2,366억 달러로 지속적으로 성장할 전망이다. 기존의 항암제는 분열이 활발히 진행되고 있는 세포의 각종 대사경로에 개입하여, 핵산의 합성을 억제하거나 세포 독성을 일으켜 항암활성을 나타내는 약제가 대부분이며, 암세포에만 선택적으로 작용하는 것이 아니라 정상세포, 특히 세포 분열이 활발한 조직 세포에도 손상을 입혀 구토, 위장장애, 탈모증, 골수기능저하로 인한 백혈구 감소증 등 심각한 부작용을 초래할 수 있다. 따라서 1세대 항암제인 세포독성(cytotoxic) 약물 대신 정상세포의 손상을 최소화할 수 있는 표적지향성을 가지는 표적 항암제의 이용이 확대되고 있으며, 대형 시장(미국, 일본, 영국, 독일 등)에서도 지속적으로 시장이 확대되고 있다. 표적 항암제들은 대부분 암세포가 특징적으로 가지고 있는 분자를 표적으로 하는데 암세포의 신호전달경로(signal transduction pathway), 혈관신생(angiogenesis), 세포간질(matrix), 세포주기조절인자(cell cycle regulator), 세포사멸(apoptosis) 등을 주요한표적으로하고 있으며, 이중 신호전달경로 억제제와 신생혈관생성 억제제가 가장 대표적인 표적 항암제로 사용되고 있다. 또한 최근 주목을 받고 있는 면역항암제의 경우 인체의 면역기능을 강화시켜 간접적으로 암을 치료한다는 점에서 기존의 치료제와는 다른 새로운 개념의 혁신적인 치료제로 각광을 받고 있으며 GBI 리서치에 따르면, 세계 면역항암제 시장규모는 매년 23.9% 성장을 통해 2017년 169억 달러에서 2022년 758억 달러까지 성장할 것으로 전망하고 있다. 다만, 암세포를 인식할 수 있는 항원 수용체의 선택성과 민감도에 따라 과도한 면역반응으로 인한 부작용이 발생할 수 있음이 한계점으로 남아있다. 이에 따라, 글로벌 제약사는 면역항암제의 한계점을 극복하고, 활용을 확대하기 위한 방법으로 2017년부터 병용요법 임상시험을 진행하고 있으며 최근에는 면역항암제와 세포독성, 표적항암제, 방사선요법 등과의 병용 요법에서 생존율 개선 등에 효과가 있다는 연구결과가 속속 발표되며 병용요법이 새로운 치료의 패러다임으로 자리를 잡고 있는 상황이다.
의약품 시장조사기관 IMS에 따르면 작년 글리벡 등 표적 항암제들의 매출 상승세가 눈에 띄게 증가했다. 유방암치료제 허셉틴, 비소세포폐암치료제 이레사, 림프종(혈액암)에 사용되고 있는 맙테라 등은 약 29~39% 매출이 상승하였으며, 간암표적항암제 넥사바, 대장암치료제 아바스틴도 약 10% 내외 매출이 성장하였다. 특히, pharmexec에 따르면 위암치료제시장의 경우 2014년 약11.3억 달러에서 2024년 약 43.9억 달러로 CAGR14.6%의 성장률을 보일 것으로 전망하였으며, 이는 전체 항암제 시장의 예상 성장률 CAGR8%를 훌쩍 뛰어넘는 수치로 위암시장이 빠르게 확대될 것을 예상하고 있다. HLB의 파이프라인으로 알려진 리보세라닙(중국명: 아파티닙)은 신생 혈관 형성을 막아 치료하는 항암제로 혈관내피세포수용체(Vascular Endothelial Growth Factor Receptor 2, VEGFR-2)의 저분자 억제제로 2세대 표적항암제에 해당한다. 약효가 탁월하고 부작용이 경쟁제품 대비 적어 글로벌 시장에서 큰 기대를 받고 있고, 중국 시장에서 이미 검증을 거친 바 있다. 2014년 중국 헝루이제약에서 위암 3차 치료제로 출시된 이후 현재까지 꾸준한 양적 성장을 이뤄내 약효와 안정성을 입증하였다. 중국 현지 증권사 레포트 및 헝루이제약 공시에 따르면 리보세라닙 (중국명: 아파티닙)의 매출은 2015년 3억 위안 (한화 약 500억원)에서 2018년17억위안(한화 약 2,900억원)으로 증가하였다. 그 밖에, 2020년 12월 간세포암 2차 치료제로 중국내 판매 승인을 득해 중국 내 매출은 지속적으로 증가할 것으로 예상된다.
6. 에이치엘비 강점과 단점
2세대 항암제인 표적치료제(Molecularly targeted therapy)는 정상세포와 암세포를 모두 공격할 수 있는 세포독성항암제와는 달리 암세포에 있는 특정 단백질 (표적)을 차단하여 암세포의 활동을 억제하는 약제로써 1세대인 세포독성 항암제에 비하여 부작용이 적은 장점을 가지고 있다. HLB가 권리를 보유한 리보세라닙은 2세대 표적항암제이면서 경구용이라는 복용 편의성을 확보했고, 부작용 또한 적어 병용치료제로 좋은 조건을 갖추고 있다. 실제로도, 기존 치료제들과의 다양한 병용요법으로 임상 연구결과들이 발표되고 있는 점 또한 앞으로의 성장성이 기대가 되는 부분이다. 리보세라닙(중국명 아파티닙)은 2014년 위암 3차 치료제로 중국 내 판매 승인을 받은후 2020년 12월 간암 2차 치료제로 중국 내 시판 승인을 받았을 뿐만 아니라 비소세포폐암, 유방암, 난소암, 등 다양한 적응증을 대상으로 임상시험이 진행 되고 있어,향후 적응증 확대에 따른 매출증가가 및 가치의 상승으로 이어질 것으로 전망하고 있다. 그리고, 중국 지역 외 나머지 글로벌 판매 권리는 에이치엘비의 자회사인 엘레바가 보유하고 있다. 엘레바에서는 간암 1차, 위암 2차, 선양낭성암, 대장암 3차 등 적응증 확대를 위해 다방면으로 힘쓰고 있다.
7. 에이치엘비 주가전망

에이치엘비의 최근 주가차트를 보자 아름답다 3월 최저점 29,900원대비 79%로 상승하였다.

에이치엘비의 지난 실적들을 보자. 다른 바이오 주식처럼 힘든 실적을 보이고 있다. 하지만 필자는 에이치엘비의 마지막 한방을 믿고 있다. 필자의 개인적인 지인은 에이치엘비 목표가를 666,000원 으로 보고 있다. 목표가를 향하여 발전하는 에이치엘비가 되었으면 좋겠다.
지금까지 글로벌 바이오 의약품 전문회사 에이치엘비에 대해 알아보았다.
* 이 포스팅은 절대 종목 추천이 아닙니다 투자의 선택은 개인의 선택이며 모든 투자의 책임은 투자자 개인에게 있습니다 *
* 공감하기와 댓글 그리고 구독하기는 필자에게 큰 힘이 됩니다*
* 이 포스팅과 다른의견 또는 건의사항 있으시면 바로 댓글부탁 드리겠습니다*
'금융투자 > 주식이야기' 카테고리의 다른 글
| 진원생명과학 주가전망 Feat. 진원생명과학 주가하락이유 (0) | 2021.08.31 |
|---|---|
| 2차전지 대장주 LG화학 주가전망 Feat. LG화학 주가하락 이유 (0) | 2021.08.29 |
| 엔씨소프트 주가전망 Feat. 엔씨소프트 주가하락 이유 (0) | 2021.08.27 |
| 수소차 관련주 대장주 TOP13 :: 총정리 (0) | 2021.08.25 |
| 크래프톤 주가전망 Feat. 크래프톤 주가하락 이유 (0) | 2021.08.12 |